कार्बन एवं इसके यौगिक karbon-carbon tatha iske yogik Important Q & A 2025

कार्बन तथा इसके यौगिक प्रश्न उत्तर : carbon aur uske yogik – 5 important Q & A 2025. Bihar Board Matric pariksha 2025 carbon – karbon tatha uske yaugik महत्वपूर्ण लघु उतरिय एवं दीर्घ उतरिय प्रश्न उत्तर मेट्रिक परीक्षा २०२५ carbon tatha iske yaugik all type question answer in hindi pdf download for clas 10th students.बिहार बोर्ड मेट्रिक परीक्षा 2025 Very – Very Important Q & A
1. कार्बनिक यौगिक किसे कहते है? उदाहरण दें | अथवा हाइड्रोकार्बन क्या है इनके उदाहरण दें |
उत्तर – ऐसे तत्व जिनमे कार्बन पाया जाता है, और जिसमें सामान्यतः कार्बन व हाइड्रोजन (C – H) के बंधन मौजूद होते हैं कार्बोनिक यौगिक कहे जाते हैं | जैसे – मीथेन , एथेनाल आदि
Q 2. कार्बनिक यौगिक का हमारे जीवन में क्या महत्व है ?
उत्तर – कार्बनिक यौगिक हमारे जीवन बहुत ही महत्वपूर्ण पदार्थ है क्योंकि सभी जीवधारियों के शारीर कार्बनिक यौगिक से ही बना है और यह हमारे भोजन में कार्बोहायड्रेट , प्रोटीन एवं वसा के रूप में पाया जाता है जो शारीरिक व मानशिक स्वस्थ का निर्माण में सहायक है | इसका उपयोग हमारे जीवन कई प्रकार से होता है जैसे – दवाइयों का निर्माण , इंधन के रूप में उपयोग और प्लास्टिक आदि जैसी आवश्यक चीजो का निर्माण में किया जाता है |
Q 3. कार्बनिक यौगिक के सूत्र लिखने कि विधि को लिखें |?
उत्तर – कार्बनिक यौगिक के सूत्र को तीन तरह से लिखा जाता है जो निम्न लिखित है –
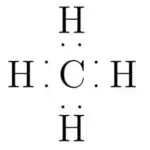
(i) लुईस इलेक्ट्रॉन डॉट संरचना (Lewis Electron Dot Structure) परिभाषा: वह संरचना जिसमें किसी अणु के संयोजक (valence) इलेक्ट्रॉनों को बिंदुओं (डॉट) के रूप में परमाणुओं के चारों ओर दिखाया जाता है, लुईस इलेक्ट्रॉन बिंदु (डॉट) संरचना कहलाती है।
उदाहरण:– मीथेन (CH₄)
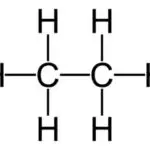
(ii) संरचनात्मक सूत्र (Structural Formula)
परिभाषा:
वह सूत्र जो किसी अणु में उपस्थित परमाणुओं की आपसी व्यवस्था तथा उनके बीच बने रासायनिक बंधों को एक रेखा (–) द्वारा स्पष्ट रूप से दर्शाता है, संरचना सूत्र कहलाता है।
उदाहरण: एथेन (C₂H₆) → H₃C—CH₃
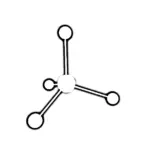
(iii) त्रि-आयामी सूत्र (Three Dimensional Formula / 3D Formula)
परिभाषा:
वह सूत्र जो अणु में परमाणुओं की वास्तविक त्रि-आयामी (3D) व्यवस्था ( लंबाई, चौड़ाई और ऊँचाई) कि स्थिति को दर्शाता है, त्रि-आयामी सूत्र कहलाता है।
उदाहरण:
मीथेन (CH₄) की टेट्राहेड्रल संरचना।
कार्बन तथा इसके यौगिक प्रश्न उत्तर : carbon aur uske yogik important Q & A 2025. लघु उतरी
Q 4. क्रियाशील मूलक क्या है ?
- उत्तर – किसी कार्बन यौगिक में पाए जाने वाले वह समूह जिस पर यौगिक का रासयनिक गुण निर्भर करता है , उस यौगिक को क्रियाशील समूह मूलक कहा जाता है
Q 8. संतृप्त हाइड्रो कार्बन और असंतृप्त हाइड्रोज कार्बन क्या है एक एक उदाहरण दें
- संतृप्त हाइड्रोकार्बन (Saturated Hydrocarbons):
वे हाइड्रोकार्बन जिनमें कार्बन परमाणुओं के बीच केवल एकल आबंध (Single Bond) होता है, उन्हें संतृप्त हाइड्रोकार्बन कहते हैं। इन्हें ऐल्केन (Alkane) भी कहा जाता है।
ये रासायनिक रूप से कम क्रियाशील होते हैं। उदाहरण: मिथेन – एथेन – - असंतृप्त हाइड्रोकार्बन (Unsaturated Hydrocarbons):
वे हाइड्रोकार्बन जिनमें कार्बन परमाणुओं के बीच द्वि-आबंध (Double Bond) या त्रि-आबंध (Triple Bond) होता है, उन्हें असंतृप्त हाइड्रोकार्बन कहते हैं।
डबल बॉन्ड वाले को ऐल्कीन (Alkene) तथा ट्रिपल बॉन्ड वाले को ऐल्काइन (Alkyne) कहते हैं। ये संतृप्त हाइड्रोकार्बन की तुलना में अधिक क्रियाशील होते हैं।
उदाहरण: एथीन – (डबल बॉन्ड) एथाइन – (ट्रिपल बॉन्ड)
Q 9. प्रकार्यात्मक समूह (Functional Group) क्या है?
उत्तर – कार्बनिक यौगिकों में उपस्थित वह विशेष परमाणु या परमाणुओं का समूह,
जो उस यौगिक के रासायनिक गुणों को निर्धारित करता है, उसे प्रकार्यात्मक समूह (Functional Group) कहते हैं। उदाहरण: –OH → अल्कोहल (Alcohol) –CHO → एल्डिहाइड
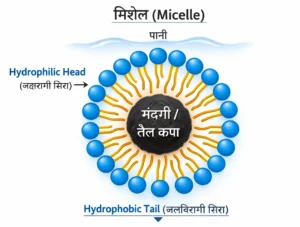
Q. मिशेल (Micelle) क्या है?
कार्बन तथा इसके यौगिक प्रश्न उत्तर : carbon aur uske yogik important Q & A 2026. लघु उतरी
- उत्तर:- जब साबुन को पानी में घोला जाता है, तो उसके अणु आपस में मिलकर एक गोलाकार संरचना बना लेते हैं। इसे मिशेल कहते है
इस संरचना में साबुन के अणु का जलविरागी (Hydrophobic) सिरा अंदर की ओर, अर्थात् गंदगी/तेल की ओर रहता है,
और जलरागी (Hydrophilic) सिरा बाहर की ओर, अर्थात् पानी की ओर रहता है।
इस प्रकार बनी गोलाकार संरचना को मिशेल (Micelle) कहते हैं।
Q 11. कार्बन के अधिक संख्या में यौगिक बनाने के दो कारण लिखें।
कार्बन के अधिक संख्या में यौगिक बनाने के मुख्य दो कारण निम्नलिखित हैं—
- शृंखलन (Catenation):
कार्बन परमाणु आपस में सह-संयोजक बंधन बनाकर लंबी, शाखित तथा वलयाकार श्रृंखलाएँ बनाने की अद्भुत क्षमता रखते हैं।
2. चतु:संयोजकता (Tetravalency):
कार्बन की संयोजकता 4 होती है, इसलिए यह चार अन्य परमाणुओं के साथ स्थिर बंधन बनाते है |
यही कारण है कि कार्बन अधिक संख्या में बंधन बनाते हैं
Q. 12 हाइड्रोजनीकरण (Hydrogenation) क्या है? इसका औद्योगिक उपयोग लिखें।
उत्तर –
असंतृप्त हाइड्रोकार्बन (जैसे वनस्पति तेल) में निकेल (Ni) उत्प्रेरक की उपस्थिति में हाइड्रोजन गैस को जोड़कर उसे संतृप्त हाइड्रोकार्बन (जैसे वनस्पति घी) में परिवर्तित करने की क्रिया को हाइड्रोजनीकरण (Hydrogenation) कहते हैं।
औद्योगिक उपयोग: –
इस प्रक्रिया का उपयोग वनस्पति तेल से वनस्पति घी (डाल्डा) बनाने में किया जाता है।
Q 13. साबुनीकरण (Saponification) किसे कहते हैं?
उत्तर:
जब किसी भी तरह के वसा या तेल को सोडियम हाइड्रोक्साइड (NaOH) के साथ गर्म किया जाता है, तो साबुन और ग्लिसरॉल बनते हैं।
इस रासायनिक अभिक्रिया को साबुनीकरण (Saponification) कहते हैं।
तेल / वसा + सोडियम हाइड्रोक्साइड → साबुन + ग्लिसरॉल उदाहरण के रूप में:
Glyceryl tristearate + NaOH → Sodium stearate + Glycerol
Q. 14. इथेनॉल का उपयोग दवाओं के निर्माण में क्यों किया जाता है?
उत्तर:
इथेनॉल एक उत्कृष्ट विलायक (Solvent) है तथा यह पानी के साथ पूर्णतः मिश्रणशील होता है।
इसी गुण के कारण इथेनॉल का उपयोग टिंचर आयोडीन, कफ सिरप, टॉनिक तथा विभिन्न औषधियों के निर्माण में किया जाता है, क्योंकि यह दवाओं के घटकों को अच्छी तरह घोलकर उन्हें प्रभावी बनाता है।
15. प्रश्न: एस्टरीकरण (Esterification) अभिक्रिया क्या है?
उत्तर:
जब एथेनॉइक अम्ल (Acetic acid) किसी उत्प्रेरक (आमतौर पर सान्द्र सल्फ्यूरिक अम्ल) की उपस्थिति में एथेनॉल के साथ अभिक्रिया करता है, तो मीठी गंध वाला पदार्थ एस्टर बनता है।
इस रासायनिक क्रिया को एस्टरीकरण (Esterification) कहते हैं।
रासायनिक समीकरण:
CH₃COOH + C₂H₅OH → CH₃COOC₂H₅ + H₂O
Q 16. साबुन और अपमार्जक (Detergent) में कोई दो अंतर लिखें।
उत्तर:
1. साबुन कठोर जल (Hard water) में सफाई के लिए उपयुक्त नहीं होता, जबकि अपमार्जक कठोर जल में भी प्रभावी ढंग से सफाई करता है।
2. साबुन वनस्पति तेलों से बनता है, जबकि अपमार्जक पेट्रोलियम के हाइड्रोकार्बन से बनते हैं।
Q 17. कार्बन न तो C^(4+) धनायन और न ही C^(4-) ऋणायन क्यों बनाता है?
उत्तर –
कार्बन न तो धनायन बनाता है और न ही ऋणायन, क्योंकि येचार इलेक्ट्रॉन त्यागने के लिए बहुत अधिक ऊर्जा की आवश्यकता होती है और
चार इलेक्ट्रॉन ग्रहण करने पर परमाणु अस्थिर हो जाता है।
इसलिए कार्बन आयन न बनाकर सहसंयोजक बंधन बना लेता है।
Q 18. हीरा और ग्रेफाइट दोनों कार्बन से बने हैं, फिर भी उनके भौतिक गुणों में भारी अंतर क्यों है?
- उत्तर – हीरा और ग्रेफाइट दोनों कार्बन से बने हैं, परंतु उनके परमाणुओं की संरचना एवं बंधन व्यवस्था अलग-अलग होती है।
इसी भिन्न संरचना के कारण उनके भौतिक गुणों में भारी अंतर पाया जाता है।
Q 19. हिरा कठोर जब्कि ग्रेफाईट मुलायम होते है क्यों ?
उत्तर :-
हीरे में प्रत्येक कार्बन परमाणु चार अन्य कार्बन परमाणुओं से मजबूत सहसंयोजक बंधन द्वारा जुड़ा होता है, जिससे यह बहुत कठोर होता है।
जबकि ग्रेफाइट में कार्बन परमाणु परतों में जुड़े होते हैं और परतों के बीच कमजोर आकर्षण बल होता है, इसलिए ग्रेफाइट मुलायम होता है।
Q 20. कठोर जल (Hard Water) में साबुन झाग क्यों नहीं देता?
उत्तर :-
कठोर जल में कैल्शियम (Ca) और मैग्नीशियम ( Mg) के लवण होते हैं जो साबुन के साथ अभिक्रिया करके अघुलनशील पदार्थ (Scum) बनाते हैं। इस कारण साबुन कठोर जल में झाग नहीं देता।
Q 21. निम्न का IUPAC नाम लिखें ? CH₃ – Cl, C₂H₅ – OH, CH₃ – CHO, CH₃ – COOH, CH₃ – CO – CH₃
| यौगिक का सूत्र | IUPAC नाम |
|---|---|
| (CH_3–Cl) | Chloromethane (क्लोरोमीथेन) |
| (C_2H_5–OH) | Ethanol (एथेनॉल) |
| (CH_3–CHO) | Ethanal (एथेनल) |
| (CH_3–COOH) | Ethanoic acid (एथेनोइक अम्ल) |
| (CH_3–CO–CH_3) | Propanone (प्रोपेनोन) |
Q 22. एल्कोहल और कार्बोक्सिलिक अम्ल में अंतर लिखें ?
| आधार | एल्कोहल (Alcohol) | कार्बोक्सिलिक अम्ल (Carboxylic Acid) |
|---|---|---|
| कार्यात्मक समूह | –OH | –COOH |
| सामान्य सूत्र | R–OH | R–COOH |
| स्वाद | कड़वा | खट्टा |
| अम्लीय प्रकृति | कमज़ोर अम्लीय | अधिक अम्लीय |
| लिटमस पर प्रभाव | कोई परिवर्तन नहीं | नीला लिटमस लाल करता है |
| उदाहरण | एथेनॉल (C₂H₅OH) | एथेनोइक अम्ल (CH₃COOH) |
Q 23. हिरा और ग्रेफाईट में अंतर स्पष्ट करें ?
| आधार | हीरा (Diamond) | ग्रेफाइट (Graphite) |
|---|---|---|
| संरचना | प्रत्येक कार्बन चार कार्बन परमाणुओं से जुड़ा होता है | प्रत्येक कार्बन तीन कार्बन परमाणुओं से जुड़ा होता है |
| बंध की प्रकृति | बहुत मजबूत सहसंयोजक बंध | परतों के बीच कमजोर आकर्षण बल |
| कठोरता | अत्यधिक कठोर | मुलायम |
| विद्युत चालकता | विद्युत का कुचालक | विद्युत का सुचालक |
| उपयोग | आभूषण, काँच काटने में | पेंसिल, इलेक्ट्रोड बनाने में |
Q 24. एथेनॉल (Ethyl Alcohol) बनाने की विधि और इसके उपयोग लिखें |
उत्तर –
एथेनॉल बनाने की विधि :-
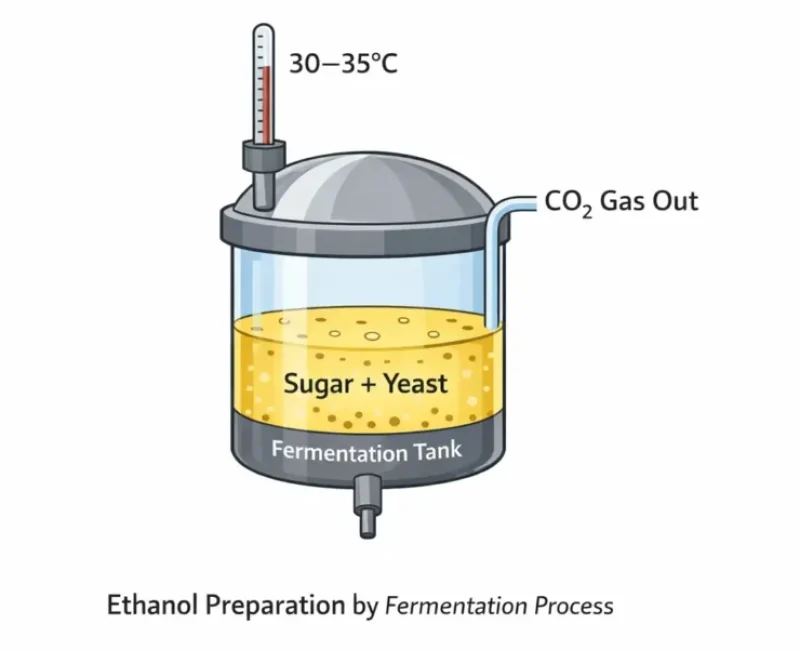
एथेनॉल का निर्माण मुख्यतः किण्वन विधि (Fermentation Process) द्वारा किया जाता है। इस प्रक्रिया में गन्ने का रस, गुड़ या शर्करा को पानी में घोलकर उसमें यीस्ट (खमीर) के मिश्रण को वायुरुद्ध पात्र में लगभग 30–35°C तापमान पर कुछ दिनों तक रखते है।
यीस्ट में उपस्थित एंजाइम शर्करा को विघटित करके एथेनॉल और कार्बन डाइऑक्साइड में बदल देता है।
रासायनिक समीकरण :
किण्वन के बाद प्राप्त घोल में एथेनॉल की मात्रा कम होती है, इसलिए उसे आसवन (Distillation) विधि द्वारा शुद्ध किया जाता है। इस प्रकार शुद्ध एथेनॉल प्राप्त होता है।
एथेनॉल के उपयोग
- एथेनॉल का उपयोग औषधि उद्योग में
- रोगाणुनाशक के रूप में घावों की सफाई में,
- ईंधन के रूप में (पावर अल्कोहल),
- पेंट, वार्निश, इत्र और कॉस्मेटिक उद्योग में
- प्रयोगशालाओं में एक उत्तम विलायक के रूप में किया जाता है।